来源:健识局
7月11日,国家药监局药审中心发布《人乳头瘤病毒疫苗临床试验技术指导原则(试行)》,放宽了HPV疫苗的临床试验标准。这是自2016年国内迎来首款进口HPV疫苗以来,监管部门第一次明确发布的指导原则,基本透露了接下来国内HPV疫苗产业链的变动逻辑。
其中,最为市场关注的是《指导原则》对迭代HPV疫苗获批上市时间上的“优待”,这意味着国产HPV疫苗或将更快上市。
市场认为,这一政策的细微改变,就是为了让国内疫苗企业有更多机会挑战全球HPV疫苗王者默沙东。
2022年年报中,默沙东披露其HPV疫苗部分总营收达68.97亿美元,同比增长22%。这部分增长多源于美国以外地区,尤其是增加了供应的中国。
众所周知,中国9价HPV疫苗处于供不应求状态已经很多年,2022年默沙东突然在中国销售放量,其实是有原因的。
世卫发出“消除宫颈癌”的口号后,疫情影响了国内的相关进程,疫情结束后的2023年是个重要开端,今年1月份,国家多部门联合发布《关于印发加速消除宫颈癌行动计划(2023—2030年)的通知》。
眼下,HPV疫苗的临床试验指导原则已经出台,种种迹象表明,HPV疫苗国产化是大方向。默沙东显然也注意到这一条,一场暗战正在进行。
临床最快只要1年,患者随访起码6年
本次公布的指导原则,将至关重要的确证性临床试验的临床设计环节,分为了第一代疫苗和迭代疫苗两部分。这一动向的主要作用,就是加快迭代疫苗的上市。
简单来说,HPV疫苗以对抗几种HPV病毒来分类,2价就是对抗两种HPV病毒,价次越高,预防的HPV病毒种类越多。当然最普通的2价疫苗是最好开发的,9价甚至更高价次的疫苗开发难度大。
按照最新的《指导原则》,企业首次研发的HPV疫苗为第一代疫苗,迭代疫苗是企业基于第一代疫苗研发平台开发的疫苗。与第一代疫苗相比,迭代疫苗的生产设备/设施、生产工艺、工艺过程控制、质量标准等与第一代疫苗原则上相同或高度相似。而且为鼓励HPV疫苗研发,“迭代疫苗可在一定程度上简化或加速临床试验”。
如何加速呢?
《指导原则》指出,如果上一代疫苗采用公认组织病理学终点,完成了保护力试验并符合上市要求,迭代疫苗可接受以病毒学终点12个月高危型持续感染(PI12)申报上市。
高危型持续感染,即是指患者处于致子宫颈等癌症的高风险病毒亚型环境下。这是观察疫苗作用的试验要求环境。《指导原则》最新的要求:一般情况下,PI12定义为在相隔5-7个月采集的人体相关成分中,连续3次及以上经PCR发现同一HPV型别核酸阳性。
这意味着,迭代疫苗最快可在12个月的临床试验后就申报上市。这种速度在10多年前是难以想象的。
2009年2月,默沙东的四价HPV疫苗在国内开启了Ⅲ期临床试验。默沙东对这一试验的预期为3年,但到2014年试验都没能结束。原因正是评价预防性疫苗的“有效终点”存有争议:为了确保安全,当时食药监局要求不仅观察到持续的HPV感染,还要真正出现癌症或发生2级以上癌变。但通常的实际状况下,患者从HPV感染,进展为子宫颈癌,一般需要10~20年。
如果等10年后真的在对照组里出现了宫颈癌后再去确定疫苗有效性,默沙东HPV疫苗可能根本就批准不了。最后,在市场较大的诉求下,几款进口HPV疫苗才被批准在中国上市。
眼下,药监局的“放松”,实际上是近10年的应用观察、以及国内产业技术积累叠加下的成果。
当然,药监局还要求HPV疫苗开展上市后的受试者随访等工作,随访应至少持续至全程免后 72 个月,鼓励更长期的有效性和安全性观察。但最关键的上市步骤,药监局显然开了口子。
万泰、沃森,靠的住么?
《指导原则》一经发出就引发市场热议,其中市场最期待的,无疑是布局HPV疫苗已久的万泰生物。
万泰生物的二价HPV疫苗已于2020年获批上市,九价HPV疫苗也正处于Ⅲ期临床中,正好能享受“迭代疫苗”的审批优势。
不过,在万泰生物最新披露的投资者会议记录中,有机构提问其二价HPV疫苗产能能否用于九价HPV疫苗,万泰生物的回应是:公司暂时无法将二价HPV疫苗生产线用于九价HPV疫苗生产。
或许,迭代疫苗要求较严的生产设备/设施、生产工艺、工艺过程控制、质量标准等方面,万泰生物未必符合要求。
另一个国内重要的HPV疫苗选手沃森生物也有机会占领优势。沃森的HPV疫苗板块主要在其子公司上海泽润。2022年上海泽润的二价HPV疫苗获批上市,在这一年获得批签发498.05万剂。以公开价格每剂329元来算,泽润这一年产的二价HPV疫苗营收16.39亿元,远低于万泰生物。
沃森生物虽然也在研发九价HPV疫苗,但进度较慢。据其披露,2022年9月份启动了与默沙东九价HPV疫苗的对比试验,生产条件等自然也还没被考虑到,能否享受迭代疫苗的福利也难说。
虽然万泰和沃森都有点悬,但已经是国内最有希望享受“迭代疫苗”政策的了。其他企业基本都是直接研发高价次疫苗,希望毕其功于一役。
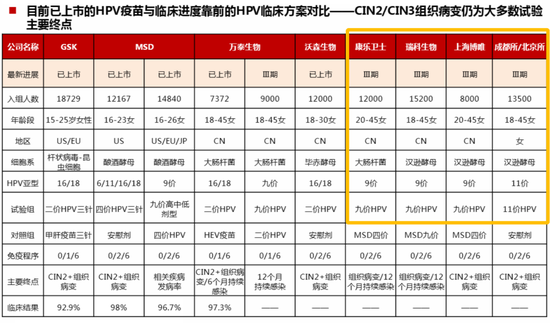
今年1月份西南证券发布的研报显示,国产九价以上HPV疫苗进入到Ⅲ期临床的至少有5家,万泰之外,康乐卫士、瑞科生物、上海博唯、成都所/北京所均对HPV市场跃跃欲试。这些企业来说,后续研发迭代疫苗的可能性偏小。
二价苗已经可以70%预防患子宫颈癌,《指导原则》指出:应慎重考虑研发更高价次疫苗的科学性与必要性。
对于独家供应的默沙东/智飞生物来说,中国这块市场份额即将被瓜分只是时间问题,唯一能做的,就是不断扩大疫苗的受众。2022年8月,默沙东九价HPV疫苗的受众扩展至9~45岁女性;今年7月11日,CDE显示,默沙东四价HPV疫苗新适应症申报上市申请已获受理…
大战马上开始
